Attraverso ulteriori sviluppi, la vetrificazione si prospetta promettente per ampie applicazioni nella ricerca sulla medicina rigenerativa.
La crioconservazione – il processo di raffreddamento e conservazione di cellule e tessuti a temperature estremamente basse, per preservarne la funzionalità e consentirne un utilizzo futuro – non è una tecnologia nuova, ma c’è ancora molto da esplorare e perfezionare in questo campo.
I metodi attuali utilizzano il congelamento lento, un processo che favorisce la formazione di ghiaccio, la disidratazione cellulare e un aumento degli agenti crioprotettivi (CPA), che proteggono le cellule dagli effetti dannosi del congelamento. Queste non sono le condizioni ideali per ottenere cellule crioconservate in modo impeccabile.
I ricercatori dell’Università di Tokyo utilizzano la vetrificazione, un processo che trasforma una sostanza in un solido non cristallino mediante un rapido raffreddamento. Questo raffreddamento produce risultati favorevoli nei campioni biologici, anche in quelli che in genere sono difficili da congelare e scongelare con successo. Nonostante alcune difficoltà intrinseche a questo metodo, il futuro della ricerca in medicina rigenerativa potrebbe essere notevolmente, e positivamente, influenzato dall’utilizzo della vetrificazione per la crioconservazione cellulare. I risultati sono pubblicati nella rivista PNAS Nexus.
La vetrificazione utilizza una pressione circa 2000 volte superiore a quella atmosferica per raffreddare rapidamente le cellule e al contempo inibire la formazione di cristalli di ghiaccio. Ciò richiede che una certa percentuale della concentrazione volumetrica sia costituita da agenti crioprotettivi per prevenire la formazione di cristalli di ghiaccio. Tuttavia, la citotossicità degli agenti crioprotettivi, ovvero il danno ai tessuti o alle cellule causato da tali agenti, è un aspetto da considerare nel processo di vetrificazione.
“Nel processo di vetrificazione, esiste un compromesso tra la citotossicità del CPA e la sua capacità di inibire la formazione di ghiaccio”, ha affermato il professore associato Masaki Nishikawa del Dipartimento di Ingegneria dei Sistemi Chimici dell’Università di Tokyo, che ha guidato lo studio. “Ridurre la concentrazione di CPA richiede in genere velocità di raffreddamento e riscaldamento più elevate per prevenire la formazione di cristalli di ghiaccio. Le principali sfide nella vetrificazione includono la bassa vitalità del campione causata dalla citotossicità del CPA e dai danni causati dai cristalli di ghiaccio, nonché le limitazioni nell’aumento dei volumi dei campioni.”
I ricercatori sono riusciti a ridurre la percentuale di CPA necessaria al 20-30%, rispetto al tipico 30-50% di volume riscontrato nella crioconservazione convenzionale tramite vetrificazione, utilizzando l’alta pressione durante il processo. Confrontando gli effetti del congelamento a pressione normale (NPF) con quelli del congelamento ad alta pressione (HPF), la vitalità cellulare e l’attività metabolica sono risultate inferiori nel caso del trattamento a pressione normale (NPF), mentre la formazione di cristalli di ghiaccio ha rappresentato un problema molto più rilevante nel caso del trattamento a pressione normale (NPF).
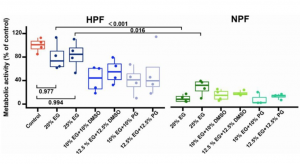
Inoltre, si sono ottenuti risultati positivi anche nel congelamento di formati cellulari complessi, come sferoidi e monostrati. Il processo di congelamento ad alta pressione si è dimostrato un metodo valido per la crioconservazione, sebbene per ottenere buoni risultati siano necessari dispositivi progettati specificamente per questo tipo di processo. I campioni trattati con HPF hanno mostrato una morfologia trasparente e priva di fratture, a dimostrazione dell’efficacia della strategia di mitigazione della formazione di cristalli di ghiaccio. Ulteriori ricerche sugli effetti della ricristallizzazione rappresentano una priorità, dato che quest’ultima può essere innescata durante lo scongelamento in queste condizioni nel ghiaccio amorfo (privo di forma). L’alta pressione utilizzata in questo metodo di vetrificazione contribuisce alla formazione di ghiaccio amorfo ad alta densità, la cui struttura non è altrettanto favorevole alla formazione di cristalli. Questo effetto potrebbe agire come un agente crioprotettivo, sebbene siano necessarie ulteriori verifiche.
L’utilizzo di tecniche complementari potrebbe consentire un processo di vetrificazione con basse o nulle emissioni di CPA. I ricercatori sperano di ottenere risultati ancora migliori combinando l’HPF con tecniche di riscaldamento avanzate durante lo scongelamento, come il riscaldamento Joule o il nanoriscaldamento. Il riscaldamento Joule utilizza l’energia elettrica per convertirla in calore, mentre il nanoriscaldamento utilizza nanoparticelle di ossido di ferro per riscaldare uniformemente l’interno.
La crioconservazione e il successivo scongelamento potrebbero trovare ampio impiego nella ricerca sulla medicina rigenerativa, consentendo di risparmiare tempo nella coltura cellulare, facilitare la standardizzazione e ridurre la variabilità tra i lotti per i test farmacologici e i trapianti cellulari.
fonte: Università di Tokyo