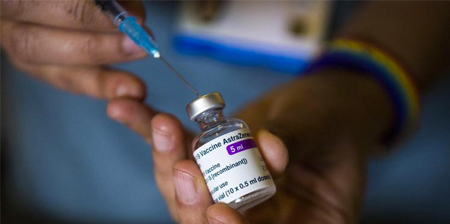
Un parere sull’autorizzazione all’immissione in commercio potrebbe essere emesso entro il 29 gennaio
L’Agenzia del farmaco europea (Ema) ha ricevuto una richiesta di autorizzazione per il vaccino anti-Covid sviluppato da AstraZeneca e dall’Università di Oxford.
L’Ema potrebbe dare una sua valutazione entro il 29 gennaio. Si tratterebbe del terzo vaccino autorizzato nell’Ue, dopo Moderna e BioNTech/Pfizer.
“Ema ha ricevuto la richiesta per l’autorizzazione condizionale alla commercializzazione del vaccino anti-Covid sviluppato da AstraZeneca e dall’università di Oxford – ha detto l’Ema – la valutazione del vaccino, noto come COVID-19 Vaccine AstraZeneca, procederà in base a una timeline accelerata possibile soltanto perché l’Ema ha già revisionato alcuni dati del vaccino nel corso della sperimentazione“.
Un parere sull’autorizzazione all’immissione in commercio “potrebbe essere emesso entro il 29 gennaio durante la riunione del Comitato per i medicinali per uso umano (Chmp), a condizione che i dati presentati sulla qualità, la sicurezza e l’efficacia del vaccino siano sufficientemente solidi e completi – si precisa nel comunicato dell’Agenzia – e che qualsiasi ulteriore informazione richiesta per completare la valutazione venga presentata tempestivamente“.
Il vaccino di Astrazeneca-Oxford ha già ricevuto il via libera delle autorità britanniche il 30 dicembre ed è stato autorizzato anche in India, Argentina, Repubblica Dominicana, Salvador, Messico e Marocco. L’Ema ha già approvato due vaccini contro il Covid-19, quello di Pfizer-BioNtech e quello di Moderna.
Come funziona il vaccino AstraZeneca
Non un vaccino ‘genetico’ a Rna come quelli di Pfizer/BioNTech e di Moderna, ma un prodotto-scudo che sfrutta un altro virus per stimolare nell’organismo difese mirate contro il coronavirus Sars-CoV-2.
Il vaccino anti-Covid di AstraZeneca – spiega l’ente regolatorio Ue – agisce preparando il corpo a proteggersi dall’infezione da Sars-CoV-2, patogeno che per entrare nelle cellule bersaglio usa proteine dette Spike presenti sulla propria superficie. Mentre i vaccini di Pfizer e di Moderna – già autorizzati dall’Ema – impiegano l’Rna messaggero (mRna) che racchiude l’informazione genetica necessaria alla produzione della proteina Spike del coronavirus, il prodotto di AstraZeneca è formato da un altro virus opportunamente modificato in modo da contenere il gene che regola la sintesi della Spike. Quello impiegato è un adenovirus reso incapace di riprodursi e che quindi non può causare malattie.
Una volta somministrato, il vaccino anti-Covid di AstraZeneca trasporta il gene di Sars-Cov-2 nelle cellule della persona al quale è stato inoculato. Le cellule useranno il gene per produrre la proteina Spike, che il sistema immunitario del vaccinato riconoscerà come un ‘nemico’ contro il quale attivare le ‘armi’ naturali rappresentate da linfociti T e anticorpi. Così, se in seguito la persona vaccinata entrerà in contatto con il coronavirus, il suo apparato immunitario lo riconoscerà e sarà pronto ad attaccarlo: anticorpi e cellule T lavoreranno insieme per uccidere Sars-CoV-2, impedirne l’ingresso nelle cellule dell’organismo e distruggere quelle infette, contribuendo in questo modo a proteggere il vaccinato da Covid-19.





